
Es el elemento principal de los compuestos orgánicos, un elemento del grupo IVA ; cuya principal característica es su capacidad de lograr enlaces muy estables y así conseguir cadenas largas de este. El silicio es otro elemento, con características similares pero no llega a formar cadenas tan largas ni tan estables como las que logra el carbono.
Este elemento se halla puro en la naturaleza en tres formas alotrópicas principalmente, estas son:
-Grafito: es una forma del carbono blanda, negra, brillante, grasosa, es buen conductor eléctrico, resistente a ciertos aspectos como el calor y algunos reactivo químicos, tiene sus átomos organizados en anillos hexagonales; cabe destacar su uso como en la creación de lubricantes, ladrillos, minas de lapices, entre otros ejemplos.

-Diamante: en este caso es una forma dura, incolora, brillante, resistente, seca , con poca conductividad eléctrica, con mayor densidad y punto de fusión. Presenta átomos establecidos en forma de tetraedro; este es usado en el comercio y en la industria como por ejemplo en la joyería, es un buen perforador y tiene la capacidad de cortar y pulir o tallar objetos duros como las gemas. Además este mismo tiene valor como piedra preciosa.

-Carbono amorfo : cuya principal característica es su baja cristalinidad. Por ejemplo esta clase de carbono lo es el hollín.

A parte de estas formas tenemos otras como los combustibles fósiles, los nanotubos, la hulla, turba, antracita, lignito, fullereno, londsdelaíta, entre otros.
El carbono posee una configuración electrónica, que permite las muchísimas probabilidades de combinarse y por consecuente formar numerosos compuestos. Su número atómico es 6 y esto indica que tiene el primer nivel lleno, en el segundo nivel logra completar el orbital 2s pero en los orbitales p, deja uno vacío y dos semillenos, lo que quiere decir que debe compartir los 4 electrones externos en enlaces covalentes, ya sean con dos átomos divalentes o con cuatro monovalentes, si bien sabemos que dos electrones pertenecen al mismo orbital 2s, aquí entra a jugar el fenómeno de la hibridación para explicar la formacion de enlaces simétricos en estos casos.
HIBRIDACIÓN: se refiere a la capacidad de mezclarse orbitales ( formando orbitales híbridos) en una nueva configuración electrónica, a la que se le llama estado excitado, con el fin de ordenar los electrones de tal forma que permitan la formación de enlaces con ciertas propiedades.
En la hibridación el tipo de enlace no es el mismo que el de orbitales no hibridados; en los hibridados tenemos enlaces sigma, formados por superposición frontal de los orbitales, posee una gran resistencia y posee alta energía; por otro lado en el caso de los no hibridados, presentan los enlaces pi, formados por superposición lateral de orbitales, son enlaces de baja energía y fáciles de romper. En cuanto a los tipos de hibridaciones tenemos 3 que son:
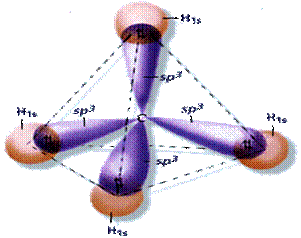
Hibridación tetragonal (sp³): presenta un enlace sencillo tipo sigma, forma enlaces de cuatro átomos monovalentes y los átomos se ubican alejados entre sí con ángulos de enlace con un valor de 109,5º.

Hibridación trigonal (sp² ): se da un doble enlace, uno tipo pi y uno tipo sigma, en este caso forma enlaces de tres átomos y los orbitales se mantienen un angulo de enlace de 120º.

Hibridación digonal(sp): se da un enlace triple, dos pi y uno sigma; solo se unen dos átomos y presentan un ángulo de enlace de 180º.

La hibridación con sus amplios ángulos de enlace ofrece una mayor estabilidad, ya que minimiza la repulsión entre electrones y los orbitales se superponen de una mejor manera.
How to make money in poker rooms: Tips and tricks to make money
ResponderEliminarHow to make money in poker rooms: Tips and tricks to make money · 1. Betting งานออนไลน์ Rules · 2. Betting Rules · 3. Trading · 4. Poker · 5. Poker.
The best casino slot machines - DRMCD
ResponderEliminarPlay at over 의왕 출장안마 500 of the hottest slot machines online for titanium wire fun or learn 제주도 출장안마 to play with confidence. We provide 화성 출장마사지 the 의정부 출장마사지 best casino slot machines for free here!